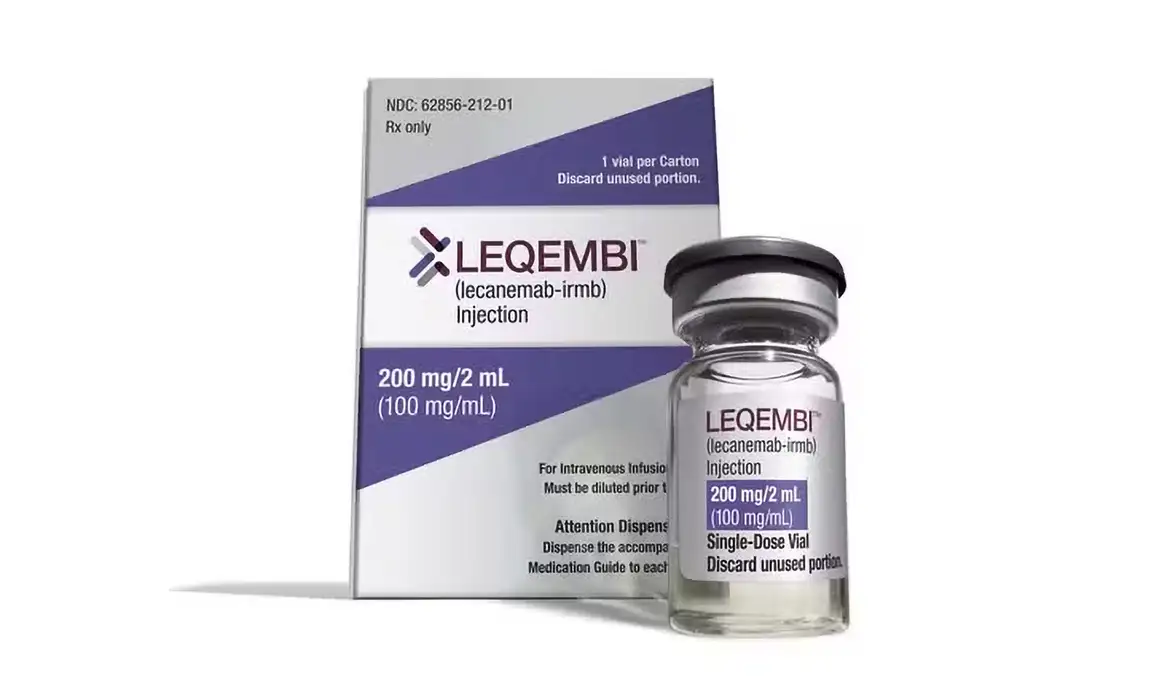
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso do medicamento Leqembi para o tratamento de pacientes diagnosticados na fase inicial da doença de Alzheimer. A liberação foi publicada no Diário Oficial da União no dia 22 do mês passado e marca a entrada de uma nova opção terapêutica voltada à demência leve associada à doença.

O Leqembi é produzido a partir do anticorpo monoclonal lecanemabe e tem como principal indicação retardar o declínio cognitivo em pessoas que já apresentam sinais iniciais do Alzheimer. O medicamento atua diretamente sobre as placas beta-amiloides no cérebro, cuja formação é considerada uma das principais características da doença.
De acordo com o registro aprovado pela Anvisa, o lecanemabe contribui para a redução dessas placas, que se acumulam entre os neurônios e estão associadas à progressão do comprometimento cognitivo. O produto é apresentado como uma solução que deve ser diluída para administração por infusão intravenosa.
A eficácia clínica do Leqembi foi avaliada em um estudo de grande porte que envolveu 1.795 participantes diagnosticados com Alzheimer em estágio inicial e com presença confirmada de placas beta-amiloides no cérebro. Os voluntários receberam o medicamento ou um placebo ao longo do acompanhamento.
Segundo a Anvisa, o principal critério de avaliação foi a mudança nos sintomas cognitivos após 18 meses de tratamento. Para isso, os pesquisadores utilizaram a escala CDR-SB (Clinical Dementia Rating – Sum of Boxes), instrumento amplamente adotado para medir a gravidade da demência em pacientes com Alzheimer.
Essa escala analisa aspectos como memória, orientação, julgamento, atividades comunitárias, tarefas domésticas e cuidados pessoais, permitindo avaliar o impacto do comprometimento cognitivo na vida diária do paciente.
No subgrupo de 1.521 pessoas analisadas com mais detalhes, os resultados indicaram que os pacientes tratados com o Leqembi apresentaram uma progressão mais lenta da doença. Eles tiveram um aumento menor na pontuação da escala CDR-SB em comparação com aqueles que receberam placebo, o que sugere um retardo no avanço dos sintomas.
A aprovação do medicamento ocorre em um contexto de busca por tratamentos capazes de interferir diretamente nos mecanismos biológicos do Alzheimer, especialmente nas fases iniciais, quando ainda há maior preservação das funções cognitivas. A Anvisa não divulgou, até o momento, informações sobre incorporação do medicamento ao Sistema Único de Saúde (SUS) ou sobre custos para os pacientes.
Com a liberação, o Leqembi passa a integrar o grupo de terapias direcionadas ao tratamento precoce da doença, abrindo novas possibilidades para pacientes diagnosticados em estágios iniciais e para profissionais de saúde que acompanham casos de demência.